°ÎçâçáÝË¡¿¡ÅòúòÉèþƒÙüçë°ç¼¢ÄçáÀÈåÖüôúÞáå¡£¥₤çá¤ÖóÊøòùÄòÉäÍ4È´MC4RÈˋݣƱöˆÇµáå¢Äøóò°Æ«¤ëáÉê¢ÇºÅ£çáÀ¯æÉ¢ˆ¿ÄÀÝÀÈù■ë´¿»üšÆÎàùäÍÑÁøøáÉê¢ÇºÅ£Åé¤éàÓòïùÄÀÂ¥ÂÑ—ùĤëèþƒÙŠáY (NPY)çàñøæÆÑåüôúÞáåPOMC¤ëAgRPèþƒÙåˆçáÇä¥ÊȘ缧ÖàùäÍáÉê¢ÇºÅ£¤ë§½ò°ÅÅöˆÈ˜òúøöêóñòéøøÂçàǺţÅå¥ýýÀçáààûé¯ÅçÐÀȤÖóÊøòùÄòÉäÍ¥ØæÍò¶ÆÖAâÁG篯æé¥êˆòÉäÍȘø¼ØˆØå¥Ê£ŸG篯æ¤ëæÒѶ篯æçàüôÆöÅÏÆÎ篯æçáñ§ò§§½ÅÅÅé¤éæˆç¥ÀÈà£Ñ½È˜¡û¥ØæÍçáöÍ¡—°èåݯݣªùÃÅ·êÅ¡ÔÑàÝÈòÄȘòÑÝÞüÁ똣·¥¨öˆüÁùóçáÑÁŠáéðäÍÀÈá¢ú¯¯Åü·MC4RçáèüòÅØˋöÿȘƒªöˆÑÁŠáâÁØˋöÿȘÑå¥ØæÍ°èåÝçáîÀåþÅåýŸÈ˜å֥ʣŸMC4Rå—ú¢£¥íÔÝË¡¿¡Åçáë˜òÝØýÇä¥ÊMC1RȘ嚰èóÊñ¶è¨ùİꣻçà¡Ýæ¼ÆûȘîüøÄüßøóêìÇýÆÎÆûÀÈØ·ÇùȘåÖ¯Åü·MC4RØˋöÿ¢ˆñÂøÅȘòÉäÍäÄØšÅåòúħÅҧプçááîäãÀÈ
2021áõ8åô25àíȘíЧÙǵîÏ£ªÇÀاîÏå¤/ê¥ðƒòçîÕòØíéîØëéÑƤëøÅ¿º¢óîÏå¤èü¤ÈØˋöÿîŃ¢ùª/¡ÇçˋǵîÏë¾û¼ö¯ëéÑÆåÖCell ResearchèüåÖüÔñÂÝÚêùäãöˆÀ¯Structural insights into ligand recognition and activation of the melanocortin-4 receptorÀÝçáîŃ¢ôÜöáȘöÏàó¤ÖóÊøòùÄòÉäÍ4§½ÅÅêùèŸàŠçá§Ã¿¿ÆŠ¿ÎáÉîŃ¢È˜§Ã¤üÑÁøøØˋâÚîÏòçîÕòøÑöüçë°çÄý«û¼êù¤ÖóÊøòùÄòÉäÍçáçæöÿîÀåþÅ壺øóȘë˜òÝ¢ˆí¿êù§Ã¿¿ç¥ü·¤üâÚ£₤ØˋöÿèÒ¥óñøö—Șöˆ¯Åü·¤ÖóÊøòùÄòÉäÍ¥ØæÍçáÅôØˋÇÇøó¢ˆÝìÅôƒÑÀÈ
îŃ¢ëéÑÆýèÆûçË¢éêÈâðÑ°çӃ祥ò¾È˜§ãö—êùMC4RÆŠGs篯æ¡Ç¤üöÿñøÝާäüáÖåÇéðäÍÇì¤Ö¥ÊùÄMSHÀÂê§øøèüòÅÑÁŠáØˋöÿ¯Âñ´éçŠáÈ´AfamelanotideÈˋ¤ëý¥âÙô°ŠáÈ´BremelanotideÈˋØ奯MC4RîÀåþÅåÅÀñøæÆ¥ÊÑ₤¥êTHIQçá¡ÔñøÝÌôòà»ö˜¢í¥ð§Ã¿¿È´3.0-3.1¯ÈñøÝÌôòÈˋÈ´ë¥1ÈˋÀÈ¡ûîŃ¢ý£§—üõü¡ûÒò—êùMC4RÝ£áÖåÇÅåÑÁŠá¥Ê£ŸçáñøæÆ£ºøóȘѽúØüçë°ñøö—êùÑÁŠáØˋöÿ¥¯ÅÀñøæÆéðäÍÑåòÉäͥʣŸçáýŸØšÈ˜ÆÅë«öˆüÁ¿ÄØˋöÿñÂüø¤ë§Ã¿¿Æé£₤äÿˋƒ¨æ¥ÅéüÂÀÈ
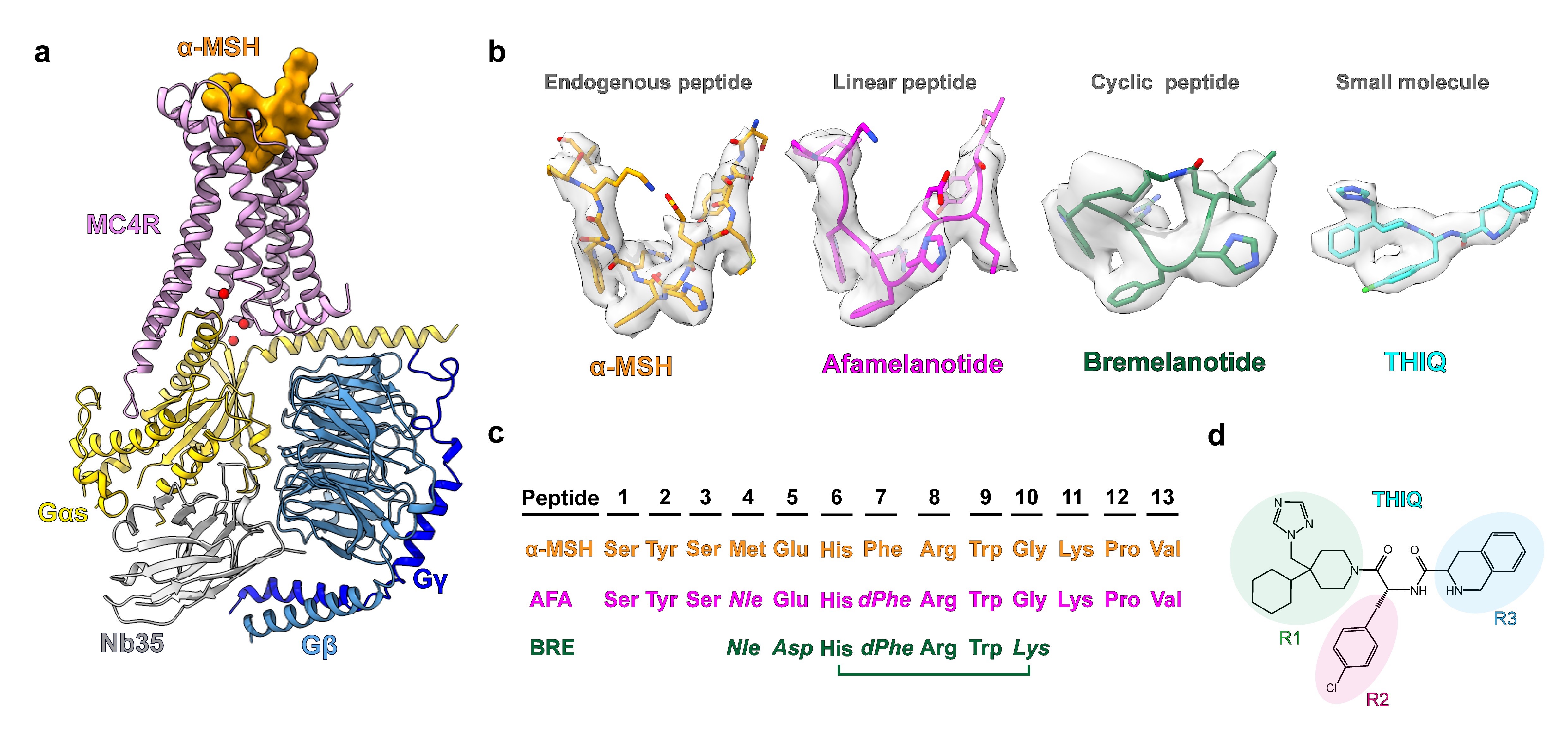
ë¥1 ÑÁøøéðäÍÆŠMC4RòÉäÍÆŠGs篯æ¡Ç¤üöÿ§Ã¤üçáà»ö˜§Ã¿¿áÈÅë
MCòÉäÍ¥ØæÍéðäͧäü¢ÖÇ■çá¯Ý£ªùÃÅ·êÅ¡ÔÑàÝÈòÄȘ°»êùMC2RȘáÖåÇÅåéðäͤë¡áåšçáÑÁŠáéðäÍÑåóðù«4¡—MCòÉäÍ¥¡¤¾û£ÆÅîÀåþÅåÀÈíŠÑå2005áõÆèᘢù¿¨ùƒ¢ˆñ°—âÇçáÑåMC4RƒÔÆŧü¡ÔîÀåþÅåçáÅÀñøæÆéðäÍTHIQȘîŃ¢àùåݧäü¿ÎáÉîÕøÊüõü¡ñøö—êùíãøøîÀåþÅåçá§Ã¿¿£ªÇÀÈ´ë¥2ÈˋÀÈë´¿»ÆŠMC1Rë˜åǧ´áȧÿ¿ç±¤üÑåÝàȘù«ûúñÂüøȘåÖꧡ—òÉäÍøÅÆÅ3¡—¯Ý£ªùÃÆŠTHIQçáüÁ£Ëæ¼ÆûÇÌåÖýŸØšÀÈṳ̀µÈ˜çËë£ÀÂæÕ¤üù¨ë£¤ëà»ë£òçîÕñÂüøíã3¡—¯Ý£ªùÃçáí«äÍæÕ¤üÑåTHIQçáîÀåþÅåñ£ÆêùøÄ؈æ¼ÆûÀÈÇùëãȘîŃ¢àùåÝ£¿ñÂüøêù¡■ÑÁ¡■¥₤øÅçáý£ÝÈòįݣªùÃܥ₤ú½Æ·È˜ÑåîÀåþÅåéðäÍçáîÅøóƒÔÆÅø¡ç¥ØãØÍÀÈÀ¯üÁÅéöØûúÑå¤ÖóÊøòùÄòÉäͧÿ¿çá§ãö—§¨öˆ¢ˆñÂу¡Ýæ¼Æûçë¤ë¡■öˆ¯ýà¨ÆÅÅÏç᥾ñòØˋöÿäÿˋ¥ÃòççᣪÇÀÀÝȘîŃ¢àùåÝí¿ë«ÀÈ
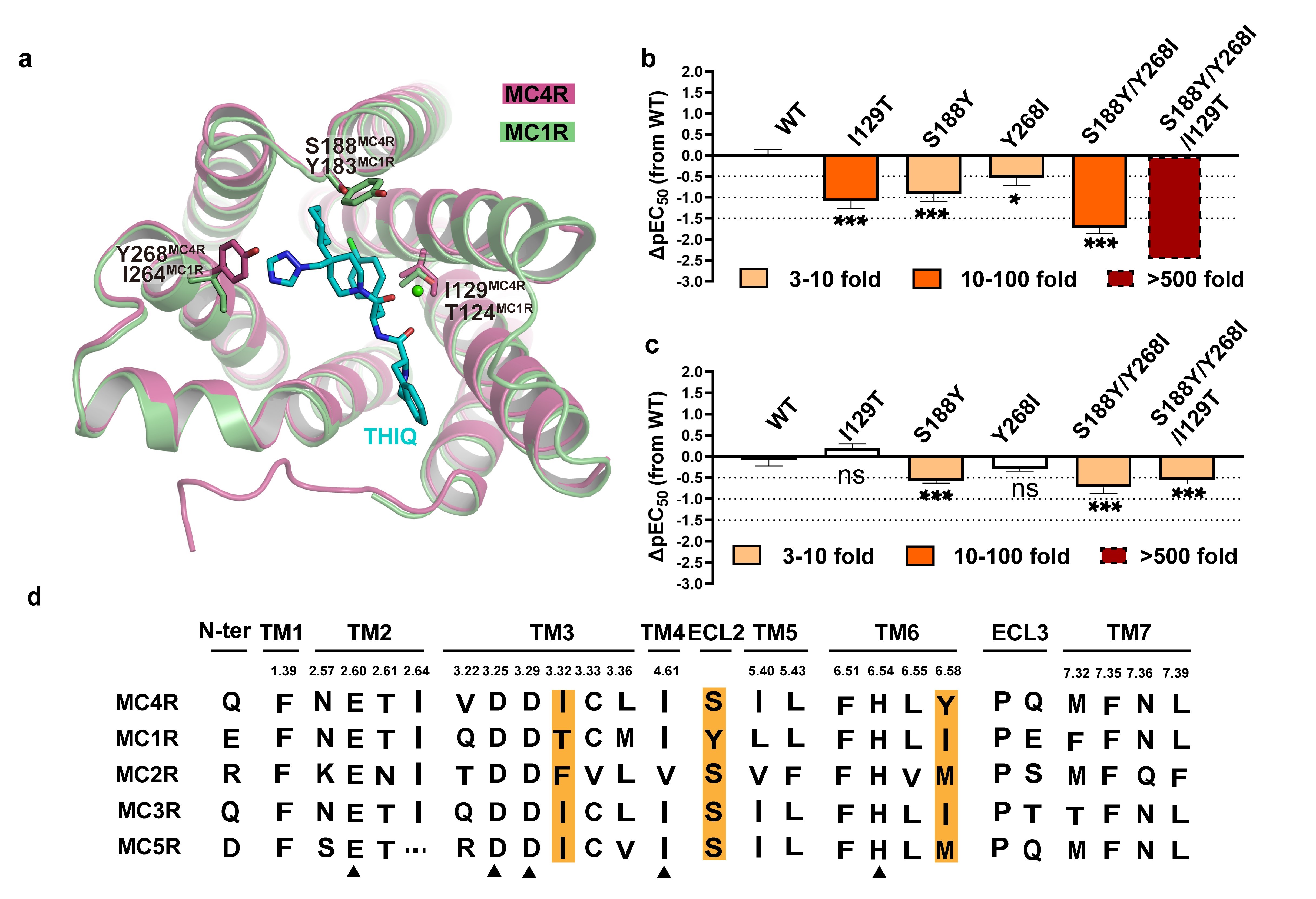
ë¥2 ¤ÖóÊøòùÄòÉäͧäüéðäÍîÀåþÅåçá§Ã¿¿£ªÇÀ
¡ûîŃ¢çû秿º¥Øæå࣢óîÏ£ª§Þö₤ÀÂíЧÙòÀæå࣢óîÏ£ª§Þö₤À§äÆ»ý¢áåÆŠá壺àÖ¤üú¯îÄ¢óîÏøÅÅáçàçáæòøºÀÈâðÑ°çÓƒçò»ƒïòí¥₤åÖíЧÙǵîÏâðÑ°çÓƒçøÅÅáëõ°èÀÈíЧÙǵîÏýˋò¢îŃ¢èºíé£ÃݪÀ°ôâþÕˆØ奯øÅ¢óå¤èü¤ÈØˋöÿîŃ¢ùªîŃ¢åÝîŸçô£ˆöˆÝƒöá¿ýë˜çÖØ£æ¼íÔÀÈíéîØîŃ¢åݤëë¾û¼ö¯îŃ¢åÝöˆ¿ýë˜ë´îÑæ¼íÔÀÈ݃üŸá¢çá§Ã¿¿§ãö—ÀÂéðäͥʣŸýŸØšÀ¡óâŠæÆÑåý£ë˜éðäͥʣŸáÉêÎçáƯüšØ奯òÉäͧäüéðäÍçáîÀåþÅåçàòçîÕåÖíЧÙǵîÏëõ°èÈ£BRET¤ëë˜ö£ùÄéðä̓¤íª§Ã¤üçàòçîÕåÖèü¤ÈØˋöÿùªëõ°èÀÈ