激素是人体的化学信使,控制着各个器官的生理功能。糖蛋白激素主要包括促黄体生成素(LH)、促卵泡激素(FSH)和绒毛膜促性腺激素(CG)三种促性腺激素,以及促甲状腺激素(TSH),参与调控下丘脑-垂体-性腺轴和下丘脑-垂体-甲状腺轴的生理功能。糖蛋白激素均为临床重要的治疗药物,其中FSH和LH用于辅助生殖及体外受精,以及治疗女性不孕症和男性促性腺功能减退症等;CG用来诱导女性排卵,增加男性精子数量等;TSH与131I联合应用于甲状腺癌术后患者,抑制和消融残余癌组织等。尽管糖蛋白激素的临床应用取得了巨大成功,但长期以来其与细胞受体的具体作用机制尚不清楚。
糖蛋白激素均由两条链(α,β)构成,其α链相同,特异β链决定受体的选择性。糖蛋白激素的受体为A类G蛋白偶联受体(GPCR)。与大多数A类GPCR不同的是,糖蛋白激素受体具有巨大的N端胞外区结构域,由约340-420个氨基酸构成,该结构域由富含亮氨酸的重复序列构成,且存在复杂的糖基化修饰,并对配体识别以及受体激活至关重要。长期以来,由于糖蛋白激素受体结构的特殊性,使得体外表达纯化该类全长受体非常困难,极大地限制了人们对于该类受体的激素选择性以及激活机制的研究。同时结构信息的缺乏也成为了靶向该类受体的小分子治疗药物研发的重大瓶颈。
2021年9月22日,浙江大学基础医学院/良渚实验室张岩研究员团队联合中国科学院上海药物研究所徐华强/蒋轶团队,共同在Nature杂志上发表了最新研究成果“Structures of full-length glycoprotein hormone receptor signaling complexes”,首次解析了全长LHCGR处于非激活以及多种激活状态下共四个结构。该工作揭示了CG与LHCGR相互作用的细节模式,阐明了受体从非激活状态到激活状态的构象变化,提出了激素配体激活受体的结构模式图,并进一步揭示了处于1期临床实验的小分子化合物Org43553与受体LHCGR相互作用细节模式,为临床开发替代激素治疗的小分子药物提供结构依据。

研究团队采用单颗粒冷冻电镜技术,首次鉴定了3种全长LHCGR的激活态结构(图1):具体包括结合内源性激素CG的LHCGR(野生型)受体结构(4.3Å)、结合内源性激素CG的LHCGR(含组成型激活突变S277I)受体结构(3.8Å)以及结合内源性激素CG和小分子化合物Org43553的LHCGR(S277I)受体结构(3.2Å)。研究首次揭示了LHCGR的全长结构,以及CG与LHCGR相互作用的细节模式。LHCGR的ECD包含11个不规则的亮氨酸折叠片,形成一个弯曲的马蹄形结构,铰链区包含一个α螺旋和第10和11亮氨酸折叠片,CG主要与受体的ECD上端结合,通过类似一种手扣手的方式与受体凹面内表面结合,CG表面与受体内表面形成电性互补。
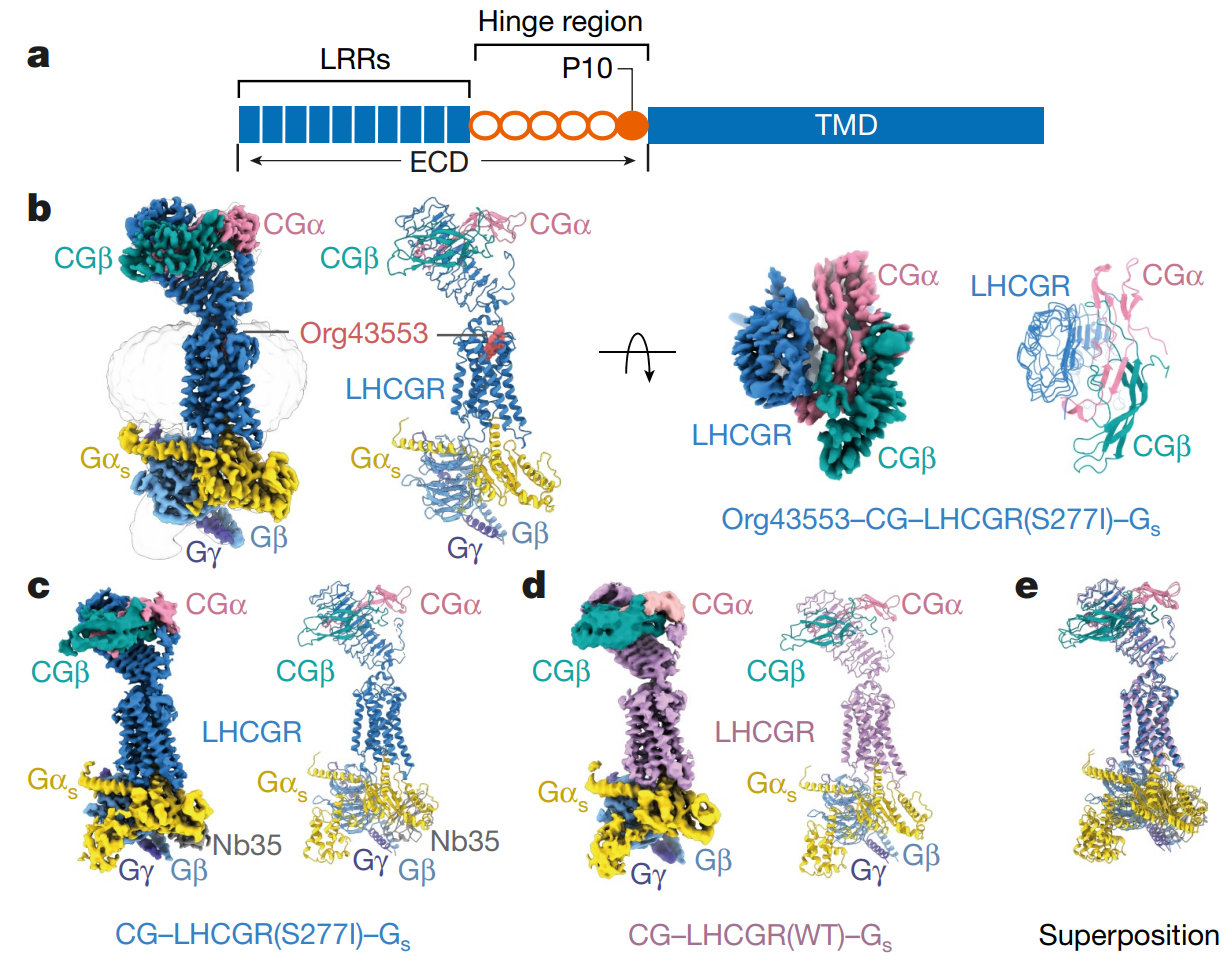
图1.糖蛋白激素受体LHCGR与CG和Gs蛋白复合物的冷冻电镜结构。
为进一步揭示LHCGR的激活机制,研究团队通过大量尝试,最终解析了全长LHCGR处于非激活状态下的电镜结构,分辨率达3.8Å。这也是目前首个报道的全长单体GPCR的电镜结构。通过受体非激活以及激活构象的对比分析,研究人员发现受体激活时ECD部分发生了~45º的偏转,进一步通过结构分析和功能试验验证,最终提出了LHCGR受体“push and pull”的结构激活模型(图2)。
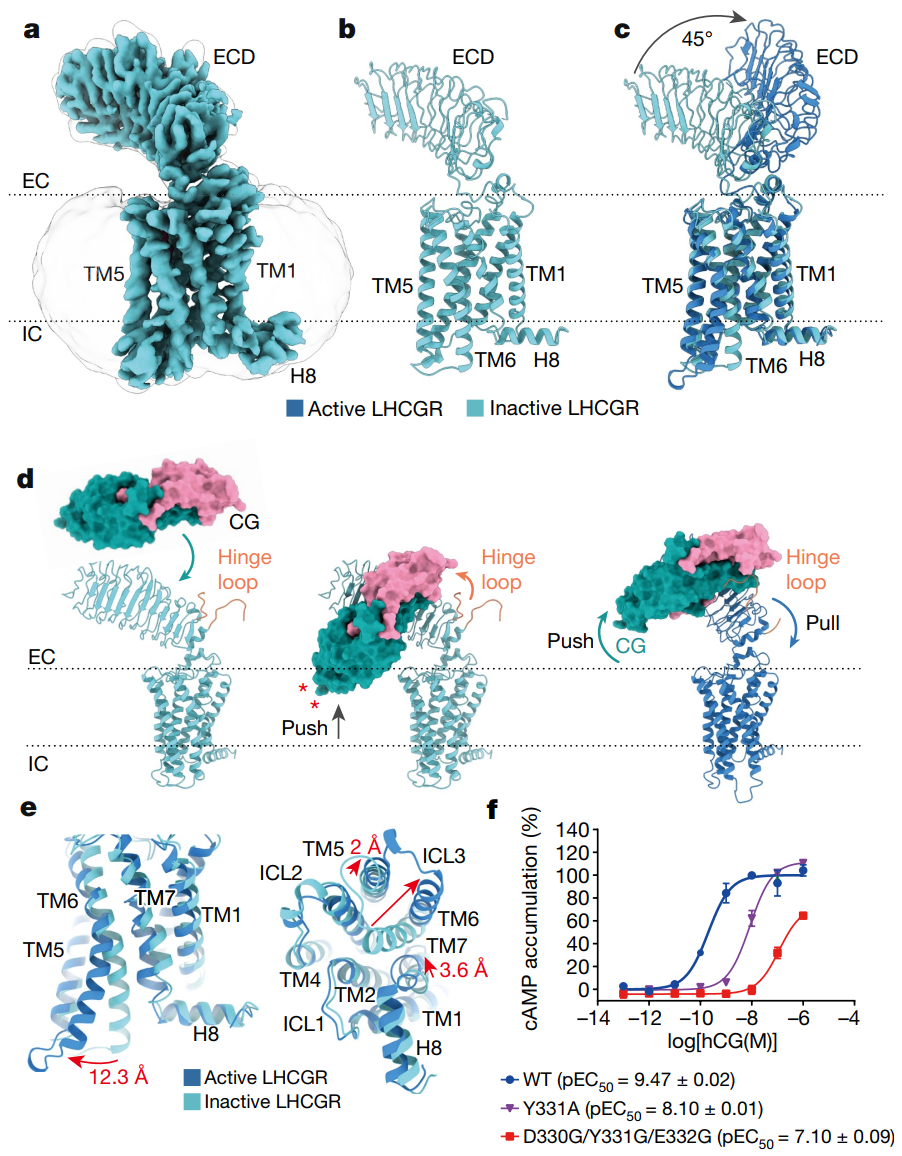
图2.糖蛋白激素受体LHCGR的激活机制。
此外,研究人员还揭示了处于1期临床实验中的小分子化合物Org43553与LHCGR精细的相互作用模式,鉴定了Org43553的结合口袋,为临床开发针对糖蛋白激素受体的选择性小分子化合物,替代激素治疗提供了结构模板。
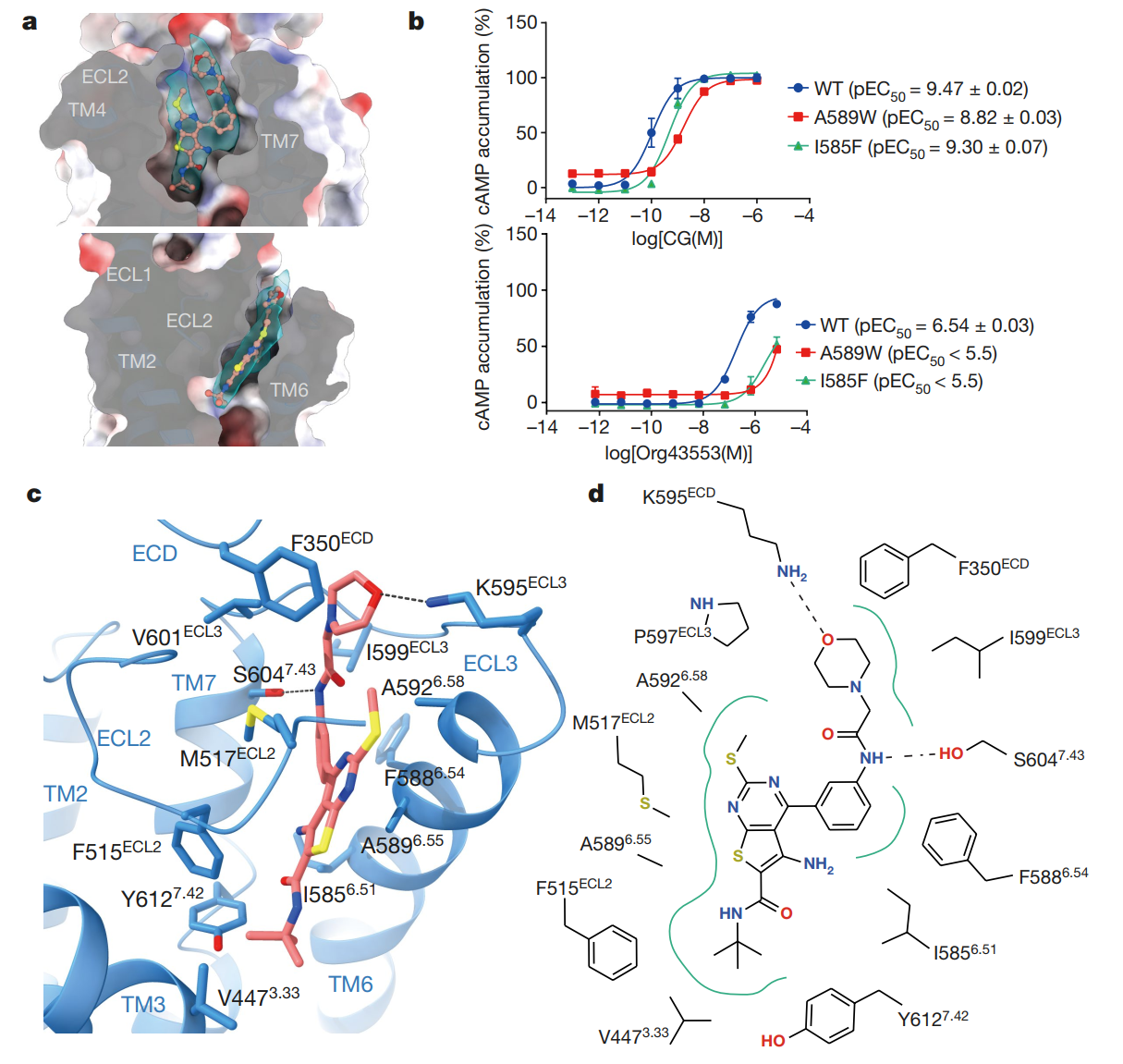
图3.小分子化合物Org43553的作用机制。
综上,本研究首次鉴定糖蛋白激素受体LHCGR的全长结构,揭示了LHCGR与其内源性激素配体CG的相互作用模式。同时也阐释了LHCGR的结构激活模型,鉴于糖蛋白激素受体结构的保守性,该激活模型同样适用于其它糖蛋白激素受体。最后,本研究进一步揭示了小分子化合物Org43553与受体LHCGR相互作用的细节模式,为靶向糖蛋白激素受体的小分子药物开发提供了结构基础。
本研究得到了国家自然科学基金委、浙江省自然科学基金委、教育部脑与脑机融合前沿科学中心等的资助。上海药物研究所博士生段佳、徐沛雨、程曦副研究员以及浙江大学医学院附属邵逸夫医院毛春友研究员为本文共同第一作者。徐华强研究员、蒋轶研究员以及张岩研究员为本文共同通讯作者。
原文链接:https://doi.org/10.1038/s41586-021-03924-2