ŇÔÂŔËÎëÄľúËŘŁ¨luzopeptinsŁ©ÎŞ´ú±íµÄ»·őĄĘ®ëÄŔࣨcyclic decadepsipeptidesŁ©Î˘ÉúÎďşĎłÉ´úĐ»˛úÎďľßÓĐC2¶ÔłĆĐԹǼܽṹˇŁËüĂÇÄÜŇÔŇ»¶¨µÄąąĎóǶČëµ˝DNAË«ÂÝĐýĎŕÁÚµÄÁ˝¸öСąµÖĐŁ¬ľßÓĐÁĽşĂµÄżąľúˇ˘żąÖ×Áöˇ˘żą˛ˇ¶ľ»îĐÔˇŁÇ°ĆÚŃĐľżŇŃ·˘ĎÖŁ¬ÂŔËÎëÄľúËŘ·Ö×ӽṹÖеÄ4-ôÇ»ů-2,3,4,5-ËÄÇâßŐŕş-3-ôČËᣨ4-OH-ThpŁ©˝áąąµĄÔŞĘǹؼüµÄҩЧÍĹŁ¬Ćä4-ôÇ»ůÉϵÄŇŇőŁ»ŻĐŢĘζÔÂŔËÎëÄľúËŘÉúÎď»îĐÔĆđľö¶¨ĐÔ×÷ÓáŁŔýČ磬˫ŇŇőŁ»ŻµÄÂŔËÎëÄľúËŘ×é·ÖAµÄżąÖ×Áöˇ˘żąľú»îĐÔ×îÇżŁ¬µ«żą˛ˇ¶ľ»îĐÔ×îČőŁ¬¶řČĄŇŇőŁ»ŻµÄÂŔËÎëÄľúËŘ×é·ÖCżą˛ˇ¶ľ»îĐÔ×îÇżŁ¬˛˘ÇŇĽ¸şőĂ»ÓĐϸ°ű¶ľĐÔˇŁÍ¬Ę±Ł¬ÂŔËÎëÄľúËؽṹÖеÄThpµĄÔŞŇ˛´ćÔÚÓÚĆäËűµÄһЩ·ÇşËĚÇĚĺëÄŔŕĚěČ»˛úÎďÖĐŁ¬ĆäϡÓĐëę»ůŁ¨hydrazoneŁ©ÉϵÄĚĽµŞË«ĽüŁ¨C=NŁ©żÉŇÔŇý·˘ëÄÁ´µÄ¦Â-ת˝Ç˝áąąŁ¬Ňň´ËThpҲĘÇŇ»ÖÖşÜÓĐÓ¦ÓĂÇ°ľ°µÄëÄÁ´˝áąąĆöżéˇŁČ»¶řŁ¬ł¤ĆÚŇÔŔ´Ł¬ÂŔËÎëÄľúËصÄÉúÎďşĎłÉ»úŔíŁ¬ĚرđĘÇThpµĄÔŞÖĐëę»ůĐγɵÄÉú»Ż»ů´ˇŇ»Ö±ĘÇŇ»¸öĂŐˇŁ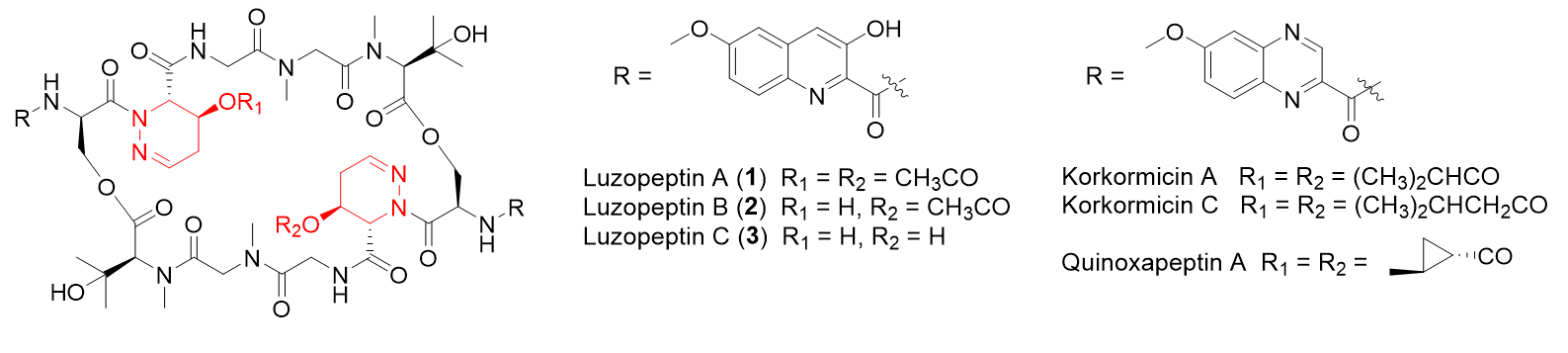
2021Äę6ÔÂ27ČŐŁ¬ąúĽĘ»ŻŃ§ÁěÓňȨÍţżŻÎAngewandte Chemie International Editionˇ·Ł¨ˇ¶µÂąúÓ¦ÓĂ»ŻŃ§ˇ·Ł©ÔÓÖľÔÚĎß·˘±íÁËŔ´×ÔŐă˝´óѧ»ů´ˇŇ˝Ń§Ôşˇ˘Őă˝´óѧҽѧԺ¸˝ĘôµÚһҽԺ¶ĹŇŐÁëżÎĚâ×éµÄŃĐľżÂŰÎġ°Enzymatic Tailoring in Luzopeptin Biosynthesis Involves Cytochrome P450-Mediated Carbon-Nitrogen Bond Desaturation for Hydrazone Formationˇ±. ÔÚŐâĎîŃĐľżÖĐŁ¬ŃĐľżŐßͨąýϵͳµÄ»ůŇňÇĂłýʵŃ顢´úĐ»ÖĐĽäĚĺ»ň¸±˛úÎ>15¸öŁ©˝áąą˝âÎöŇÔĽ°ĚĺÍâÉú»Ż·´Ó¦ÖŘąąµČʵŃ飬ϵͳ˝âÎöÁËÂí¶ĹŔ·ĹĎßľúÖĐÂŔËÎëÄľúËصÄÉúÎďşĎłÉ»úŔíŁ¬˝ŇĘľÁËŇ»ŔŕеĶ๦ÄÜϸ°űÉ«ËŘP450øLuz26˛ÎÓëëÄÁ´şóĐŢĘÎąýłĚÖĐÁůÇâßŐŕş-3-ôČËᣨpiperazateŁ©µĄÔ޵ÄC-NĽüÍŃÇâ·´Ó¦Ł¬ĐÎłÉëę»ůˇŁ´ËÍ⣬ŃĐľżŐß»ą·˘ĎÖŁ¬¶ÔÂŔËÎëÄľúËŘÉúÎď»îĐÔĆđľö¶¨ĐÔ×÷ÓõÄŇŇőŁ»ŻĐŢĘÎĘÇÓÉŇ»¸öĤ˝áşĎµÄőŁ»ůתŇĆø´ß»ŻŁ¬Í¨ąýĚĺÍâøѧ±íŐ÷Ó붨µăÍ»±äʵŃ飬ŃĐľżŐßÍƲâŐⲽ·´Ó¦ĘÇŇ»¸öżçĤŇŇőŁ»ŻąýłĚŁ¬Ľ´ŇŇőŁ¸¨Ă¸A˝«ŇŇőŁ»ůͨąýø»îĐÔÖĐĐĵĿçĤż×µŔתŇƸřŇŃתÔËÖÁ°űÍâµÄĘÜĚĺÂŔËÎëÄľúËŘ×é·ÖCˇŁŇň´ËŁ¬ŐâÖÖ˝«ÎŢϸ°ű¶ľĐÔµÄÉúÎďşĎłÉÖĐĽäĚĺĎČתŇĆÖÁ°űÍâÔŮĐŢĘγɻîĐÔÖŐ˛úÎďżÉÄÜĘÇŇ»ÖÖϸľú¶Ô×ÔÉí˛úÉúµÄżąÉúËŘÄÍŇ©µÄ»úÖơŁ
ÁíÍ⣬ĽřÓÚC-NĽüµÄČĄ±ĄşÍ·´Ó¦¶ÔÓÚP450ĽŇ×ĺŔ´ËµĘÇ·ÇłŁĎˇÓеķ´Ó¦ŔŕĐÍŁ¬ŃĐľżŐß˝řŇ»˛˝¶ÔĆä´ß»Ż»úŔí˝řĐĐÁËĚ˝ľżˇŁÍ¨ąýŇÔP450øLuz26ÎŞÖ¸µĽµÄĘýľÝżâÍÚľňŁ¬ŃĐľżŐßÔÚ˝Î÷Â×´ÄĘĎľúŁ¨Lentzea jiangxiensisŁ©µÄĹŕŃřÎďÖĐ·˘ĎÖÁËһϵÁĐş¬ßßŕ¤Ëá˝áąąµĄÔ޵ÄÂŔËÎëÄľúËŘŔŕËĆÎ˝Î÷ëÄľúËŘŁ©ˇŁ¶Ô¸ĂľúÖĐLuz26µÄͬԴµ°°×JxpK˝řĐĐһϵÁĐĚĺÄÚÓëĚĺÍâʵŃé˝áąűĚáĘľLuz26´ß»ŻµÄC-NČĄ±ĄşÍ·´Ó¦żÉÄÜĘÇĎČôÇ»ŻşóÍŃË®µÄ´ß»Ż»úŔíˇŁ
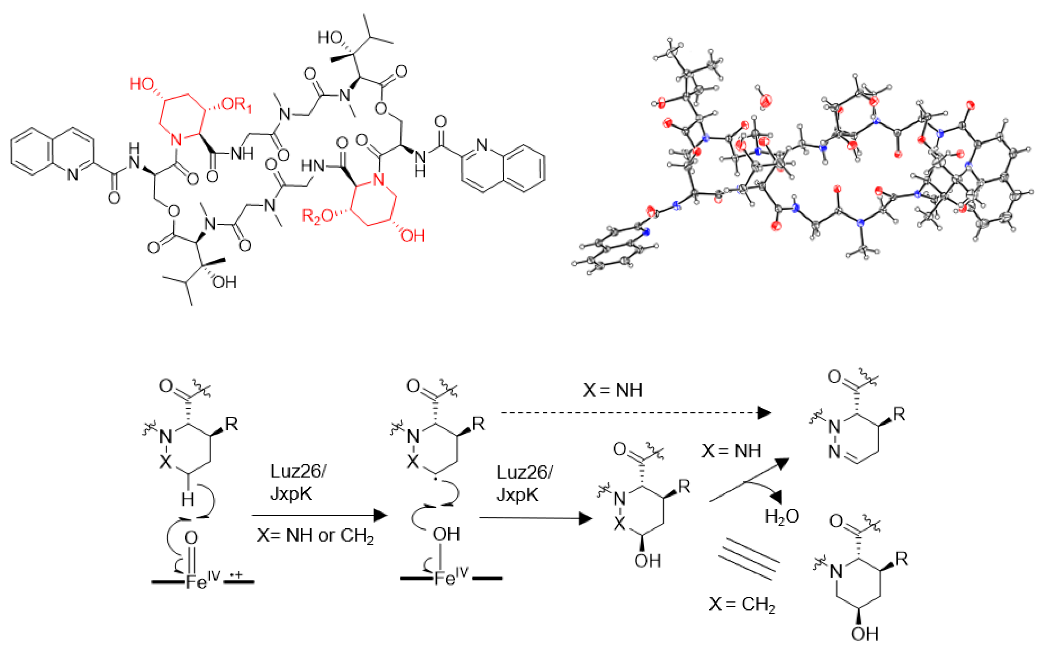
×ŰÉĎŁ¬¸ĂŃĐľż˝âÎöÁËÂŔËÎëÄľúËصÄø´ŮĐŢĘÎąýłĚŁ¬˝ŇĘľÁËThp˝áąąµÄÉúÎďşĎłÉÍľľ¶ˇŁLuz26µÄĚĽ-µŞµĄĽüÍŃÇâ»îĐÔÍŘŐąÁËϸ°űÉ«ËŘP450øµÄ´ß»Żą¦ÄÜŁ¬Luz27µÄżçĤ´ß»ŻĚáĘľÁËϸľú¶Ô×ÔÉí˛úÉúµÄżąÉúËŘÄÍŇ©µÄĐ»úŔíˇŁ´ËÍ⣬ÂŔËÎëÄľúËŘÉúÎďşĎłÉ»ůŇň´ŘµÄĽř¶¨Ľ°ŔŕËĆ»ůŇň´ŘµÄÍÚľňÓë˛úÎďĽř¶¨Î޸ĂŔ໯şĎÎď˝ńşóµÄ˝áąą¸ÄÔěÓë×éşĎÉúÎďşĎłÉµě¶¨ÁË»ů´ˇˇŁ
±ľÎĵĵÚŇ»×÷ŐßÎŞŐă˝´óѧ¶ĹŇŐÁëżÎĚâ×éµÄ˛©ĘżÉúĘ©öνܺͿĆŃĐÖúŔí»ĆÁ˘Ă÷Ł¬Í¨Ń¶×÷ŐßÎŞ¶ĹŇŐÁ롣¸Ăą¤×÷Ęܵ˝ąúĽŇÖصăŃĐ·˘ĽĆ»®şĎłÉÉúÎďѧÖصăרĎîĎîÄżˇ˘ąúĽŇ×ÔČ»żĆѧ»ů˝đÎŻĎîÄżşÍŐă˝Ęˇ×ÔČ»żĆѧ»ů˝đĎîÄżµÄÖ§łÖˇŁ
ÔÎÄÁ´˝ÓŁşhttps://onlinelibrary.wiley.com/doi/epdf/10.1002/anie.202105312