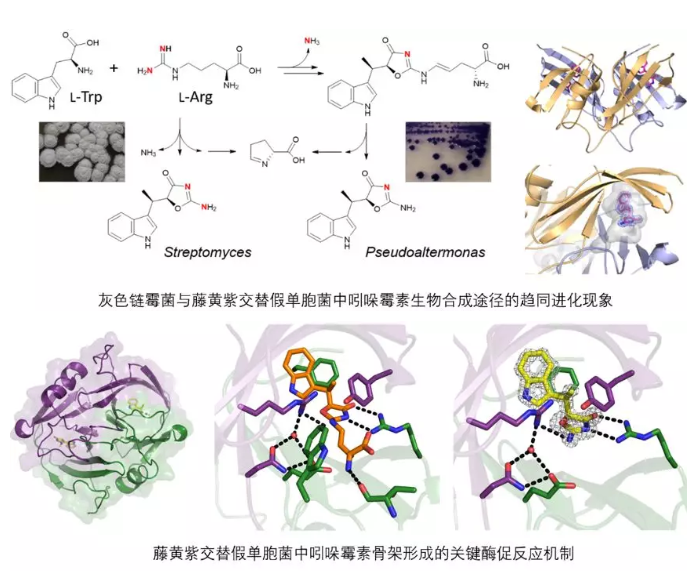
微生物与植物来源的天然产物活性分子是现代临床药物的重要来源之一,具有抗菌、抗癌、抗感染等多种生物学活性。在微生物中,此类化学结构多样与活性各异的特异性代谢产物通常是由相应的生物合成基因簇编码合成,它们发挥着包括抗菌、信号分子、金属离子载体等化学生态学作用。通常情况下,这些生物合成基因簇的进化是由趋异进化(divergent evolution)主导的。这种进化方式推动着编码小分子化学结构的多样化与分子创新,微生物也以此来适应不停变化的生境。
2019年8月12日,国际学术权威刊物自然出版集团旗下子刊《Nature Chemical Biology》杂志在线发表了来自浙江大学基础医学院、浙江大学医学院附属第一医院杜艺岭课题组与加拿大英属哥伦比亚大学化学系Katherine S.Ryan课题组的合作论文(Convergent biosynthetic transformations to a bacterial specialized metabolite)原文链接:https://www.nature.com/articles/s41589-019-0331-5。在这项研究中,研究者则通过对抗生素吲哚霉素(indolmycin)生物合成途径的系统研究,揭示了一个罕见的细菌特异性代谢过程的趋同进化(convergent evolution)现象。
吲哚霉素是一种细菌色氨酰tRNA合成酶的竞争性抑制剂,近年来发现对一些临床耐药菌具有很好的杀菌活性。在前期的工作中,研究者已经报道了来源于土壤的革兰氏阳性细菌灰色链霉菌中吲哚霉素的组装过程及其中多个新颖的生物化学反应机制(PNAS,112(9):2717-2722,2015;Nat Chem Biol, 13(8):836-838,2016)。
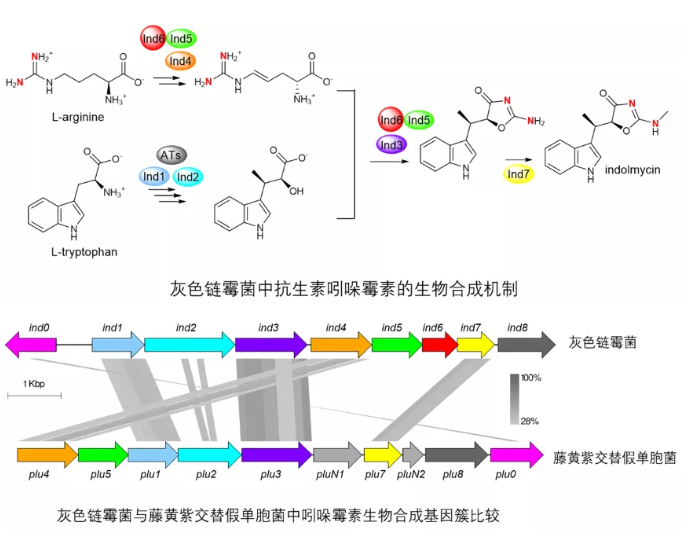
在最新的研究中,研究者通过体外生化反应重构、蛋白晶体结构解析和合成生物学等多种技术手段,对一株海洋来源的藤黄紫交替假单孢菌中吲哚霉素的合成途径进行了解析。研究结果显示以上两株系统进化远缘的细菌采用了不同的生物合成逻辑与合成酶家族来组装出同一个终产物。受到自然界中这两条不同的生物合成路线的启发,研究者通过整合三株不同细菌中的生物合成酶,构建出了一条更为高效的吲哚霉素人工合成途径。这项工作不仅揭示了一种独特的微生物天然药物生物合成过程的趋同进化现象,而且也为通过合成生物学技术实现药物优质高产提供了新的思路。杜艺岭研究员是文章第一兼共同通讯作者,博士生赵桂云为共同作者,该项工作受到了浙江大学百人计划、国家自然科学基金面上项目和浙江省杰出青年基金等项目经费的支持。