Gµ°°×ĹĽÁŞĘÜĚ壨GPCRŁ©ĘÇČËĚĺÄÚ×î´óµÄĤĘÜĚĺµ°°×ĽŇ×壬ĆäÔÚϸ°űĐźŴ«µĽÖĐ·˘»ÓÖŘŇŞą¦ÄÜŁ¬Í¬Ę±Ň˛ÓëČËĚ弲˛ˇĂÜÇĐĎŕąŘŁ¬ĘÇ40%ŇÔÉϵÄÉĎĘĐŇ©ÎďµÄ×÷Óðе㡾1ˇżˇŁ¸ůľÝ˝áąąşÍĐňÁеIJîŇěĐÔŁ¬ČËĚĺÖĐGPCRżÉ·ÖÎŞAˇ˘Bˇ˘CşÍFËÄÖÖŔŕĐ͡Ł˝üÄęŔ´µÄ˝áąąą¦ÄÜŃĐľż·Ö±đ˝ŇĘľÁËAˇ˘B1ˇ˘B2şÍFŔŕŇÔµĄĚĺĐÎĘ˝·˘»Óą¦ÄܵÄGPCPµÄĽ¤»î»úÖơľ2-5ˇżˇŁŃĐľżĎÔĘľµĄĚĺGPCRĹĽÁŞGµ°°×˛ÉÓĂĎŕËƵÄÄŁĘ˝Ł¬Ľ´ĘÜĚĺµÄĽ¤»îĘążçĤ˝áąąÓňTM6µÄÍâŇĆŁ¬˝ř¶řĐγɽϴóµÄżÚ´üÓĂÓÚ˝áşĎG¦ÁŃÇ»ůµÄCÄ©¶ËŁ¬´Ó¶řĽ¤»îGµ°°×ĎÂÓÎĐĹşĹͨ·ˇŁČ»¶řł¤ĆÚŇÔŔ´Ł¬ŇÔ¶ţľŰ»ŻĐÎĘ˝·˘»Óą¦ÄܵÄCĐÍGPCRĹĽÁŞGµ°°×µÄ·Ö×Ó»úÖĆһֱδÄÜ˝ŇĘľŁ¬ŃĎÖŘ×č°ÁËČËĂǶÔCĐÍĘÜĚĺĐĹşĹתµĽ»úÖƵÄŔí˝âˇŁ
2021Äę4ÔÂ28ČŐŁ¬»ŞÖпƼĽ´óѧÉúĂüżĆѧÓ뼼ĘőѧԺÁő˝Ł·ĺ˝ĚĘÚÍŶÓÓëŐă˝´óѧ»ů´ˇŇ˝Ń§Ôşˇ˘ÁĽäľĘµŃéĘŇŐĹŃŇŃĐľżÔ±ÍŶÓÔÚNatureÔÓÖľÔÚĎß·˘±íÁËĚâÎŞˇ°Structural basis of GABAB receptor-Gi protein couplingˇ±µÄŃĐľżÂŰÎġŁ±ľŃĐľżÍ»ĆĆĐԵؼř¶¨ÁËCĐÍŇěÔ´¶ţľŰĚĺGABABĘÜĚĺÓëGµ°°×¸´şĎÎďµÄ¸ß·Ö±ćÂĘŔ䶳µçľµ˝áąąŁ¬ÔÚĘŔ˝çÉĎĘ״νŇĘľ¶ţľŰĚĺGPCRĹĽÁŞGµ°°×µÄĐÂÄŁĘ˝ˇŁ
CĐÍGPCRÖ÷ŇŞ°üŔ¨´úĐ»ĐͦĂ-°±»ů¶ˇËáĘÜĚ壨GABABŁ©ˇ˘´úĐ»Đ͹Ȱ±ËáĘÜĚ壨mGluŁ©ˇ˘¸ĆĂô¸ĐĘÜĚ壨CaSRŁ©şÍζľőĘÜĚĺ1Ł¨Taste 1Ł©µČˇľ6ˇżˇŁCĐÍĘÜĚĺÓëÖÚ¶ŕÉńľşÍľ«ÉńĽ˛˛ˇĎŕąŘŁ¬°üŔ¨ń˛đĚŰÍ´ˇ˘˝ąÂǡ˘ŇÖÓôˇ˘ľ«Éń·ÖÁŃÖ˘ˇ˘Ň©ÎďłÉń«ˇ˘Rett×ŰşĎŐ÷şÍń˛đďĐÔÄÔ˛ˇµČˇŁGABABĘÜĚĺĘǵÚŇ»¸ö±»·˘ĎÖşÍÖ¤Ă÷µÄGPCRŇěÔ´¶ţľŰĚ壬ĘÇCĐͶţľŰĚĺGPCRµÄµäĐÍ´ú±íˇľ7,8ˇżˇŁGABABĘÜĚĺąă·ş±í´ďÔÚÖĐĘŕÉńľĎµÍłÖĐŁ¬˛ÎÓëѧϰˇ˘ĽÇŇäşÍÍ»´ĄĐźŴ«µÝµČÖŘŇŞµÄÉúŔí˝řłĚˇľ9ˇżˇŁGABABĘÜĚĺÓÉGB1şÍGB2Á˝¸öŃÇ»ů×éłÉŁ¬Ăż¸öŃÇ»ů·Ö±đÓÉ°űÍâ˝áąąÓň(VFT)Ł¬Ćß´ÎżçĤÓň(TMD)şÍ°űÄÚÓňąąłÉˇľ10ˇżˇŁGABABĘÜĚ弤»î˛ÉȡµäĐ͵ķǶԳĆĐÔµ÷˝Ú»úÖĆŁ¬Ľ´GB1µÄVFT¸şÔđĹäĚĺʶ±đŁ¬¶řGB2µÄTMĹĽÁŞGi/oµ°°×µ÷żŘĎÂÓÎĐźšŁÁő˝Ł·ĺ/ŐĹŃŇşĎ×÷ÍŶÓÔÚ2020ÄęąúĽĘĘ×´ÎĽř¶¨Č«ł¤GABABĘÜĚĺ·ÇĽ¤»î̬Ó뼤»î̬µÄľ«Ď¸ČýάżŐĽä˝áąąŁ¨ĎęĽűBioArt±¨µŔŁşŐĹŃŇ/Áő˝Ł·ĺşĎ×÷˝âÎö´úĐ»ĐͦĂ-°±»ů¶ˇËáĘÜĚ弤»î»úÖƵĽṹ»ů´ˇŁ©Ł¬˛űĂ÷ÁËGABABĘÜĚ弤»îʱµÄąąĎóת±äąýłĚŁ¬Ľř¶¨ÁËŐýĎň±äąąµ÷˝ÚĽÁµÄ˝áşĎżÚ´üŁ¬Ľ«´óµŘ´Ů˝řÁËGABABĘÜĚĺµÄĽ¤»î»úÖĆŃĐľżşÍ°ĐĎňŇ©Î↑·˘ˇŁÍ¬Ę±Ł¬¸Ăą¤×÷»ąĘ״νâÎöÁ˵ͷֱćµÄGABAB-Gi¸´şĎÎď˝áąąŁ¬·˘ĎÖÓÉÓÚDZÔڵĿռäλ×裬¶ţľŰ»ŻµÄGABABĘÜĚĺ˝öÄÜĹĽÁŞŇ»¸öGµ°°×ˇľ11ˇżˇŁČ»¶řĆä·Ç¶ÔłĆĽ¤»îşÍĹĽÁŞGµ°°×µÄĐĹşĹתµĽµÄ·Ö×Ó»úÖĆ»ąÎ´±»˝ŇĘľˇŁ
±ľŃĐľżÍŶÓÔÚÇ°ĆÚą¤×÷µÄ»ů´ˇÉĎÔٴνřĐĐżÎĚ⹥ąŘŁ¬ĎČşóÍ»ĆƸ´şĎÎď×é×°ˇ˘ľůŇ»Ŕ䶳ŃůĆ·ÖƱ¸ˇ˘¶ŻĚ¬ąąĎóĘýľÝ´¦ŔíµČĚôŐ˝Ł¬×îÖŐÍęłÉ¸ß·Ö±ćGABABĘÜĚĺ-Giµ°°×¸´şĎÎďµÄµçľµ˝áąąĽř¶¨Ł¨ÍĽ1aŁ©ˇŁ˝áąą·ÖÎö·˘ĎÖÓ뵥ĚĺGPCR˛»Í¬Ł¬GABABĘÜĚĺĹĽÁŞGµ°°×ʱŁ¬Á˝¸öŃÇ»ůżçĤÓňµÄTM6ľůĂ»ÓĐ·˘ÉúÍâŇĆŁ¬µ«ĘÇGB2ŃÇ»ůµÄTM3şÍTM5Č´·˘ĎÖ˝ĎС·ů¶ČµÄÍâŔ©Ł¬ĘąČý¸ö°űÄÚ»·ĐÎłÉŇ»¸ö˝ĎÇłµÄżÚ´ü˝áşĎGµ°°×ˇŁÓ뵥ĚĺGPCRĎŕ±ČŁ¬Gµ°°×¦Á5ÂÝĐý˛ĺČëGABABĘÜĚĺµÄÉî¶ČµÍÁˡ«10ÅŁ¬˛˘ÇŇÖ÷ŇŞÓë°űÄÚ»·»Ą×÷ˇŁŐâĐ©˝áąű˝áşĎŇÔÇ°µÄĆäËűCĐÍGPCRą¦ÄÜŃĐľżŁ¬ÍƲâCĐÍGPCR¶ţľŰĚ嶼˛ÉÓĂÁËŐâÖÖ˛»Í¬ÓÚAˇ˘B1ˇ˘B2şÍFŔŕGPCPµÄĽ¤»îµÄ¶ŔĚصÄGµ°°×ĹĽÁŞÄŁĘ˝Ł¨ÍĽ1b-dŁ©ˇŁ
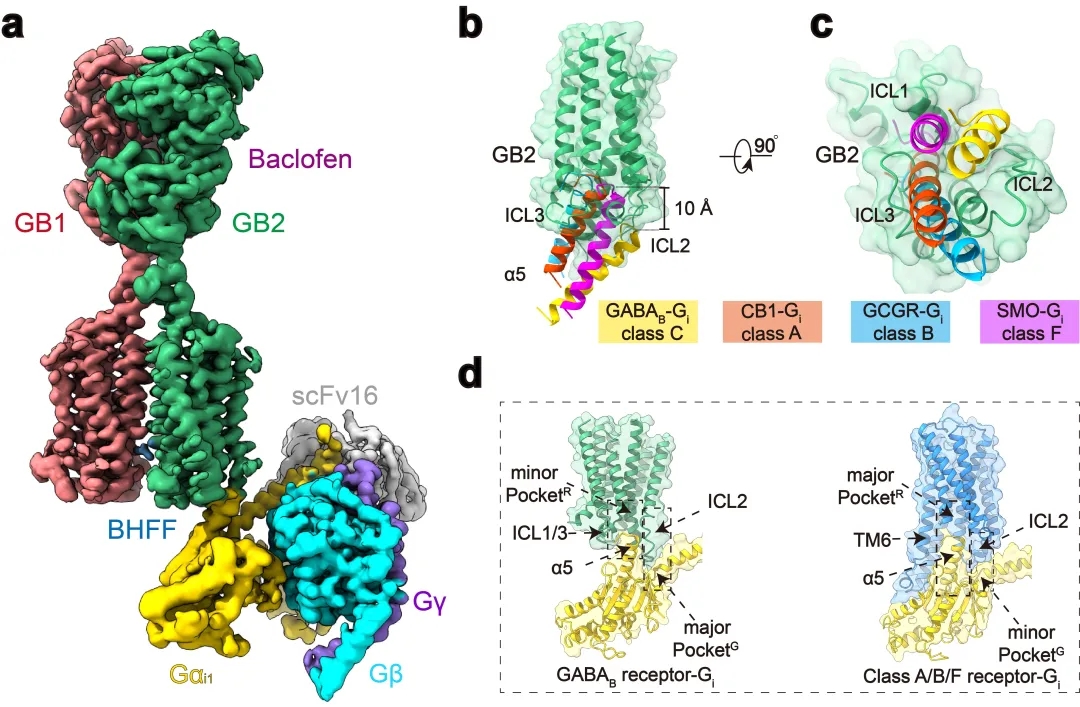
ÍĽ1ŁşGABABĹĽÁŞGµ°°×¸´şĎÎďµÄĐÂÓ±˝áąą
´ËÍ⣬ŃĐľż·˘ĎÖÁËGABABĹĽÁŞGµ°°×şóµÄľ«Ď¸ąąĎó±ä»ŻŁ¬°üŔ¨GB1şÍGB2Ö®ĽäµÄĐýתŁ¬ŇÔĽ°GB2ŃÇ»ůTMµÄϸ˝Ú±ä»ŻˇŁÍ¨ąý˝áąą·ÖÎöŁ¬ŃĐľżČËÔ±·˘ĎÖ˝áşĎĽ¤¶ŻĽÁµÄGABABĘÜĚĺĹĽÁŞGµ°°×şóŁ¬ĆäGB2-TMĎŕ˝ĎÓÚGB1-TM˛úÉú˝řŇ»˛˝µÄÄćʱŐëĐýתŁ¬ĘąµĂGB1şÍGB2µÄżçĤÓň˝çĂć˝řŇ»˛˝żż˝üŁ¬Îȶ¨Ľ¤»î״̬ˇŁŃĐľżČËԱרעÓÚGB2-TMµÄÄÚ˛żľ«Ď¸µÄąąĎó±ä»ŻŁ¬·ÖÎö·˘ĎÖGB2 TM3/TM5°űÄڶ˵ĹąĎó±ä»ŻĘÇĆđĘĽÓÚTM3ÉĎF586˛ŕÁ´±˝»·µÄ´ó˝Ç¶ČĐýתˇŁĐĹşĹתµĽĘµŃé·ÖÎö·˘ĎÖŁ¬˝«F586Í»±äłÉС˛ŕÁ´±ű°±ËáşóŁ¬ĘÜĚĺĹĽÁŞGµ°°×µÄÄÜÁ¦ĎÔÖřĎ½µˇŁ´ËÍ⣬ÔÚGB2-TMµÄµ×˛żŁ¬¶ŕ¸ö´řµçşÉµÄ°±»ůËáĐγɵÄŃÎÇĹ˝řŇ»˛˝Îȶ¨ÁËĘÜĚĺµÄĽ¤»î̬,´Ó¶ř˝ŇĘľÁËGB2ŃÇ»ů˝áşĎGµ°°×µÄ˝áąą»ů´ˇŁ¨ÍĽ2Ł©ˇŁGB2ŃÇ»ůŐâĐ©¶ŔĚصĹąĎóµÄ±ä»ŻŁ¬×îÖŐľö¶¨ÁËGABABĹĽÁŞGµ°°×µÄ·Ç¶ÔłĆĐÔĽ¤»îÄŁĘ˝ˇŁ
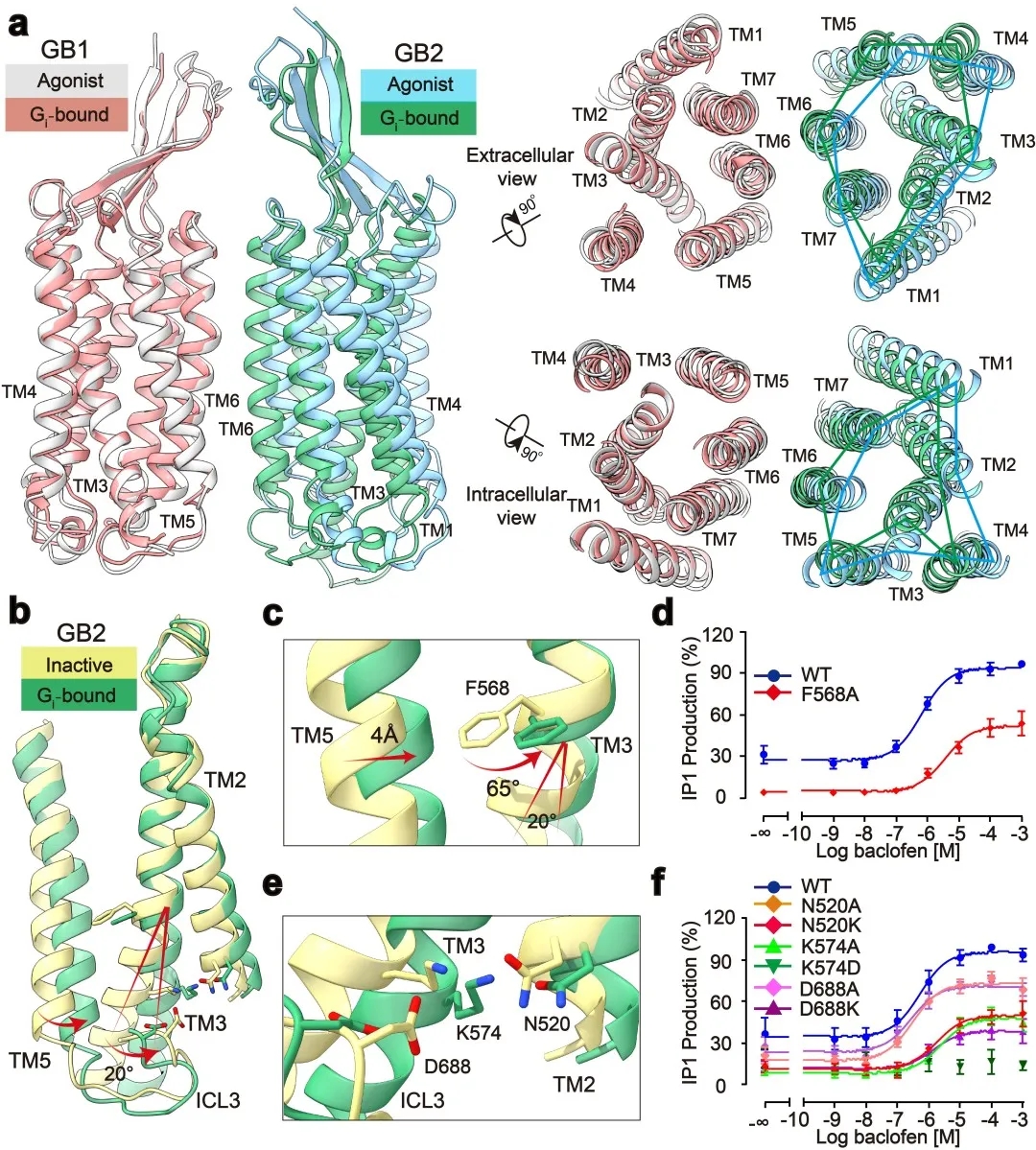
ÍĽ2ŁşGABABĘÜĚĺ˛Éȡ·Ç¶ÔłĆĐԱ仯µÄĽ¤»î»úÖĆ
GABABÖ÷Ҫͨąý3¸ö°űÄÚ»·ĹĽÁŞGiµ°°×ŁşĆäÖнϳ¤µÄICL2Ö÷ŇŞÓëGµ°°×ÉϦÁ5Ł¬¦ÁNŁ¬¦Â2-¦Â3µÄ˝áşĎŁ¬ŐĽľÝÁËÔĽ80%µÄ»Ą×÷˝çĂ棻¶ř˝Ď¶ĚµÄICL1ˇ˘ICL3Ö÷ŇŞÓëGµ°°×µÄ¦Á5Ä©¶ËĽ¸¸ö°±»ůËáĎ໥×÷ÓĂŁ¬Îȶ¨ÁËGµ°°×µÄ˝áşĎŁ¨ÍĽ3aŁ¬bŁ©ˇŁ´ËÍâŃĐľż·˘ĎÖGABABĘÜĚĺѡÔńĐÔʶ±đGi/oŃÇĐÍGµ°°×ĘÇÓÉÓÚGi/oµÄH5.23λµăĘÇС˛ŕÁ´µÄ°ëë×°±Ëᣬ¶řGsˇ˘GqµČŔŕĐÍGµ°°×µÄĎŕӦλÖĂ´ó˛ŕÁ´µÄŔŇ°±ËáÓëGABABĘÜĚĺľßÓĐDZÔڵĿռäλ×裨ͼ3cŁ©ˇŁą¦ÄÜʵŃé·ÖÎö·˘ĎÖŁ¬µ±°ŃH5.23λµăµÄ°ëë×°±ËáÍ»±äłÉ´ó˛ŕÁ´µÄÉ«°±ËáşóŁ¬ĆäĹĽÁŞGµ°°×µÄÄÜÁ¦ĎÔÖř˝µµÍŁ¬¶řµ±Í»±äłÉС˛ŕÁ´µÄ±ű°±ËáşóŁ¬Ćä˝áşĎGµ°°×µÄÄÜÁ¦Ă»Óб仯Ł¨ÍĽ3d,eŁ©ˇŁ

ÍĽ3ŁşGABABĘÜĚĺѡÔńĐÔĹĽÁŞGiµ°°×µÄ·Ö×Ó»úÖĆ
¸ĂĎ×÷ÍęŐűµŘ˛űĘöÁËCĐÍŇěÔ´¶ţľŰĚĺGABABĘÜĚĺµÄ·Ç¶ÔłĆĽ¤»î»úÖĆŁşÔÚ·ÇĽ¤»î״̬ĎÂŁ¬GABABĘÜĚĺÁ˝¸öŃÇ»ůµÄVFTÇř¶Ľ´¦ÓÚżŞ·Ĺ״̬Ł¬TMÇř˛ÉÓĂTM3-TM5/TM3-TM5»Ą×÷˝çĂ棻Ľ¤¶ŻĽÁ˝áşĎGB1-VFTŐýλżÚ´üşóŁ¬ÓŐµĽGB1-VFT±ŐşĎŁ¬´Ó¶řĘąµĂGB2-VFTĐýתŁ¬˝řŇ»˛˝ÓÉľ±Çř´«µĽÖÁTM˝áąąÓňµÄÖŘĹĹŁ¬ĐÎłÉеÄTM6/TM6×÷ÓĂ˝çĂ棻PAMŇÔĽ°Gµ°°×µÄ˝áşĎŁ¬˝řŇ»˛˝ÓŐµĽÁËGB2µÄTMÇřµÄĐýתŁ¬ĐγɸüÎȶ¨µÄTM6/TM6»Ą×÷˝çĂ棻´ËÍâGB2ŃÇ»ůF568µČ˛Đ»ůľ«Ď¸µÄąąĎó±ä»ŻŁ¬µĽÖÂĆäTM3/TM5µÄ°űÄÚ¶ËÍâŇĆŁ¬Čý¸ö°űÄÚ»·ĐγɽĎÇłµÄżÚ´üѡÔńĐÔĹĽÁŞGi/oµ°°×Ł¬×îÖŐĽ¤»îĎÂÓÎĐĹşĹͨ·Ł¨ÍĽ4Ł©ˇŁ
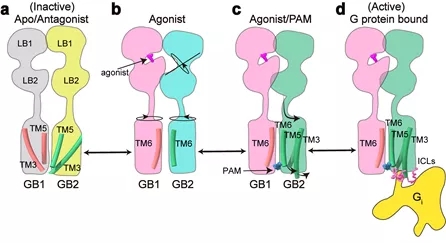
ÍĽ4ŁşGABABĘÜĚ弤»îµÄĐĹşĹתµĽÄŁĐÍ
±ľŃĐľżĘÇŐă˝´óѧˇŞ»ŞÖпƼĽ´óѧϸ°űĐĹşĹתµĽÁŞşĎʵŃéĘŇÔÚCĐÍGPCRĐĹşĹתµĽ»úÖĆŃĐľżÖеÄÓÖŇ»ÖŘ´óÍ»ĆơŁ¸Ăą¤×÷Ҳ˝řŇ»˛˝ŃéÖ¤ÁËÁő˝Ł·ĺżÎĚâ×é֮ǰ·˘ĎÖµÄCĐÍGPCR¶ţľŰĚ壬Čç´úĐ»Đ͹Ȱ±ËáĘÜĚ壨Nat Chem Biol.Ł¬2015; PNAS., 2011Ł©Ł¬GABABĘÜĚ壨Cell ResearchŁ¬2020; Nat Commun.Ł¬2019Ł»EMBO J.Ł¬2008Ł©şÍ¸ĆĂô¸ĐĘÜĚ壨PNAS.Ł¬2020Ł©Öв»Í¬ŃÇ»ůµÄ¸÷¸öą¦ÄÜÓň±äąąµ÷˝ÚµÄĽ¤»îÄŁĘ˝ˇŁ»ŞÖпƼĽ´óѧÓëŐă˝´óѧ»ů´ˇŇ˝Ń§ÔşÁŞşĎĹŕŃř˛©ĘżÉúÉę˛ÖËɡ˘Őă˝´óѧ»ů´ˇŇ˝Ń§Ôş˛©ĘżşóĂ«´şÓѡ˘»ŞÖпƼĽ´óѧ˝ĚʦĐíćżľęşÍ˛©ĘżÉú˝úéŞÎޱľŃĐľżµÚŇ»×÷ŐߡŁ»ŞÖпƼĽ´óѧÉúĂüżĆѧÓ뼼ĘőѧԺÁő˝Ł·ĺ˝ĚĘÚŁ¬Őă˝´óѧ»ů´ˇŇ˝Ń§ÔşŐĹŃŇŃĐľżÔ±şÍ·¨ąúą¦ÄÜ»ůŇňŃĐľżËůPIN JP˝ĚĘÚÎŞą˛Í¬Í¨Ń¶×÷ŐߡŁŐă˝´óѧҽѧԺµ°°×ÖĘƽ̨ˇ˘Ŕ䶳µçľµÖĐĐÄÎŞ±ľ´ÎŃĐľżµÄŃůĆ·ÖƱ¸şÍĘýľÝĘŐĽŻĚáą©ÁËÖ§łÖˇŁ¸Ăą¤×÷ҲµĂµ˝ÁËŐă˝ÖĐҽҩ´óѧłÂÖŇ˝ĚĘÚŁ¬Őă˝´óѧҩѧԺşî͢ľü˝ĚĘںͷ¨ąúą¦ÄÜ»ůŇňŃĐľżËůRondard P˝ĚĘÚµÄĐÖúˇŁ±ľą¤×÷µĂµ˝Á˿ƼĽ˛żąúĽŇÖصăŃĐ·˘ĽĆ»®ˇ˘ąúĽŇ×ÔČ»żĆѧ»ů˝đµČĎîÄżµÄ´óÁ¦Ö§łÖˇŁ
˛ÎżĽÎÄĎ×
1 Hauser, A. S., Attwood, M. M., Rask-Andersen, M., Schiöth, H. B. & Gloriam, D. E. Trends in GPCR drug discovery: new agents, targets and indications. Nature reviews. Drug discovery 16, 829-842, doi:10.1038/nrd.2017.178 (2017).
2 Rasmussen, S. G. et al. Crystal structure of the ¦Â2 adrenergic receptor-Gs protein complex. Nature 477, 549-555, doi:10.1038/nature10361 (2011).
3 Zhang, Y. et al. Cryo-EM structure of the activated GLP-1 receptor in complex with a G protein. Nature 546, 248-253, doi:10.1038/nature22394 (2017).
4 Ping, Y. Q. et al. Structures of the glucocorticoid-bound adhesion receptor GPR97-G(o) complex. Nature 589, 620-626, doi:10.1038/s41586-020-03083-w (2021).
5 Qi, X. et al. Cryo-EM structure of oxysterol-bound human Smoothened coupled to a heterotrimeric G(i). Nature 571, 279-283, doi:10.1038/s41586-019-1286-0 (2019).
6 Pin, J. P. & Bettler, B. Organization and functions of mGlu and GABA(B) receptor complexes. Nature 540, 60-68, doi:10.1038/nature20566 (2016).
7 Kaupmann, K. et al. GABA(B)-receptor subtypes assemble into functional heteromeric complexes. Nature 396, 683-687, doi:10.1038/25360 (1998).
8 White, J. H. et al. Heterodimerization is required for the formation of a functional GABA(B) receptor. Nature 396, 679-682, doi:10.1038/25354 (1998).
9 Vlachou, S. & Markou, A. GABAB receptors in reward processes. Advances in pharmacology (San Diego, Calif.) 58, 315-371, doi:10.1016/s1054-3589(10)58013-x (2010).
10 Bettler, B., Kaupmann, K., Mosbacher, J. & Gassmann, M. Molecular structure and physiological functions of GABA(B) receptors. Physiological reviews 84, 835-867, doi:10.1152/physrev.00036.2003 (2004).
11 Mao, C. et al. Cryo-EM structures of inactive and active GABA(B) receptor. Cell research 30, 564-573, doi:10.1038/s41422-020-0350-5 (2020).