细胞自噬(Autophagy)是一个高度保守的真核细胞维持稳态的生物学过程。自噬在多种生理和病理过程中扮演重要的角色,自噬的失调与多种人类疾病密切相关,例如癌症、神经退行性疾病、糖尿病、传染性疾病等。按照底物特异性的有无,自噬可以分为非选择性自噬(non-selective or bulk autophagy)和选择性自噬(selective autophagy)。以特定蛋白受体介导的、能够识别并降解特异性底物的自噬,被称为选择性自噬(selective autophagy)(1)。
内质网(endoplasmic reticulum, ER)是单层膜结构的细胞器,参与细胞内很多关键的生命活动过程,包括蛋白合成、分泌、脂合成以及钙离子的储存等等。ER失稳与多种重大疾病密切相关,因此维持ER稳态的分子机制一直是生命科学的研究热点(2)。有意思的是,ER不仅是自噬起始的关键场所,同时也是自噬的底物,以ER为特异性底物的自噬称为内质网自噬(ER-phagy)。ER-phagy的缺失能导致遗传性感觉神经元障碍症(HSAN-II)等疾病(3, 4)。在细胞中,ER通常形成一个完整的网络状结构,而自噬小体的直径一般在0.5-1.5微米之间,因此ER-phagy发生必须具备的一个前提条件是:待降解的ER被片段化成合适的大小(‘bite-sized’ pieces),才可能被自噬小体包裹起来,进而和溶酶体融合后降解。近几年,数个ER-phagy受体陆续被鉴定,这些工作极大地促进了人们对ER-phagy的理解。但是,ER膜结构如何被片段化;ER片段化如何与自噬小体的识别和包裹耦合;ER-phagy的选择性受体如何特异性识别待降解的ER而不作用于ER的其他部分;ER-phagy是如何响应上游调控信号等等重要生物学问题尚待解答。
2020年1月13日,浙江大学基础医学院孙启明、Dante Neculai和南京大学医学院方雷团队在《EMBO J》上发表题为" FAM134B oligomerization drives ER membrane scission for ER-phagy"的研究论文(5)。该研究发现ER-phagy受体蛋白FAM134B(3)通过其RTN结构域相互作用而发生同源寡聚化,这一过程以目前尚且未知的方式诱导ER膜片段化。随后,片段化的ER膜凭借FAM134B与LC3的直接互作被自噬小体识别并包裹。该研究还发现内质网应激(ER stress)能升高细胞质Ca2+浓度,激活钙调蛋白依赖的CAMK2B激酶,后者通过直接磷酸化FAM134B RTN结构域中的Ser151显著促进多聚体化和ER膜片段化效率。因此,CAMK2B-FAM13B信号轴确保在内质网应激条件下细胞通过提高ER-phagy活性以应对内质网应激胁迫。该研究还提供了另外一个实验证据支持其科学假设,他们发现一个来自HSAN-II病人的突变体FAM134BG216R表现出异常多聚体化和过量ER膜片段化,并诱导过度的ER-phagy和感觉神经元死亡。
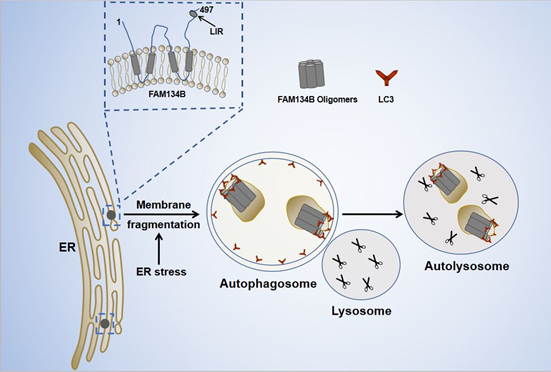
FAM134B的多聚体化在内质网自噬中的功能示意图
该研究提出了ER膜片段化的动态调节模型,从而为ER-phagy的时空调控提供了进一步的机制性见解。过度ER-phagy导致感觉神经元死亡这一发现不仅从另一个侧面揭示了适度的自噬在维持细胞和机体稳态中的必要性,还可能为HSAN-II患者的临床诊断和治疗提供重要理论基础和实践依据。浙江大学医学院生物化学系、浙江大学附属第二医院心脏医学系博士后江肖和博士研究生王心怡、丁贤明为文章第一作者,浙江大学基础医学院、浙江大学附属第二医院孙启明,浙江大学基础医学院、浙江大学院附属邵逸夫医院Dante Neculai和南京大学医学院方雷为本文的共同通讯作者。中科院生物物理所胡俊杰研究员提供了RTN4 cDNA;浙江大学医学院公共实验平台、浙江大学电镜中心为本项目的实施提供了大力支持。本课题受国家自然科学基金以及科技部蛋白质机器重大研发计划等项目资助。