核苷(酸)类似物是抗病毒药物中最重要的结构家族,它们中包括了最新的抗新冠病毒药物莫努匹拉韦(Molnupiravir)和瑞德西韦(Remdesivir)等。这些小分子在体内能够转化为其对应的活性三磷酸形式进而干扰病毒复制等正常的生理过程。氮-氮(N-N)化学键是天然及化学合成来源核苷类分子的一个重要结构基团(图1),但目前对氮-氮键在自然界中的形成过程知之甚少,其酶促合成的生物化学分子基础也是当前微生物合成代谢领域最前沿的科学问题之一。
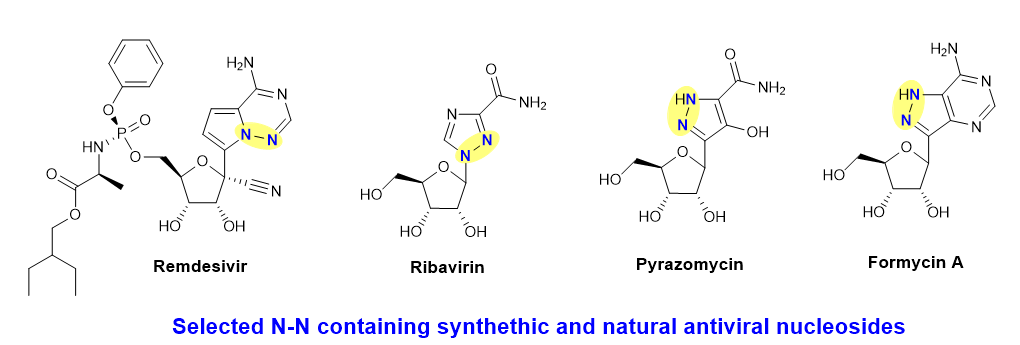
2021年12月10日,国际学术权威刊物《Nature Communications》杂志在线发表了来自浙江大学医学院附属第一医院/基础医学系杜艺岭课题组的研究论文“Molecular basis of enzymatic nitrogen-nitrogen formation by a family of zinc-binding cupin enzymes”。在这项研究中,研究者通过对微生物来源的天然抗病毒分子吡唑霉素(pyrazomycin)中氮-氮键基团形成的生化机理的研究,揭示了一类锌离子依赖型氮-氮键合酶介导肼基(-NH-NH-)形成的详细生化过程和催化机理(图2)。
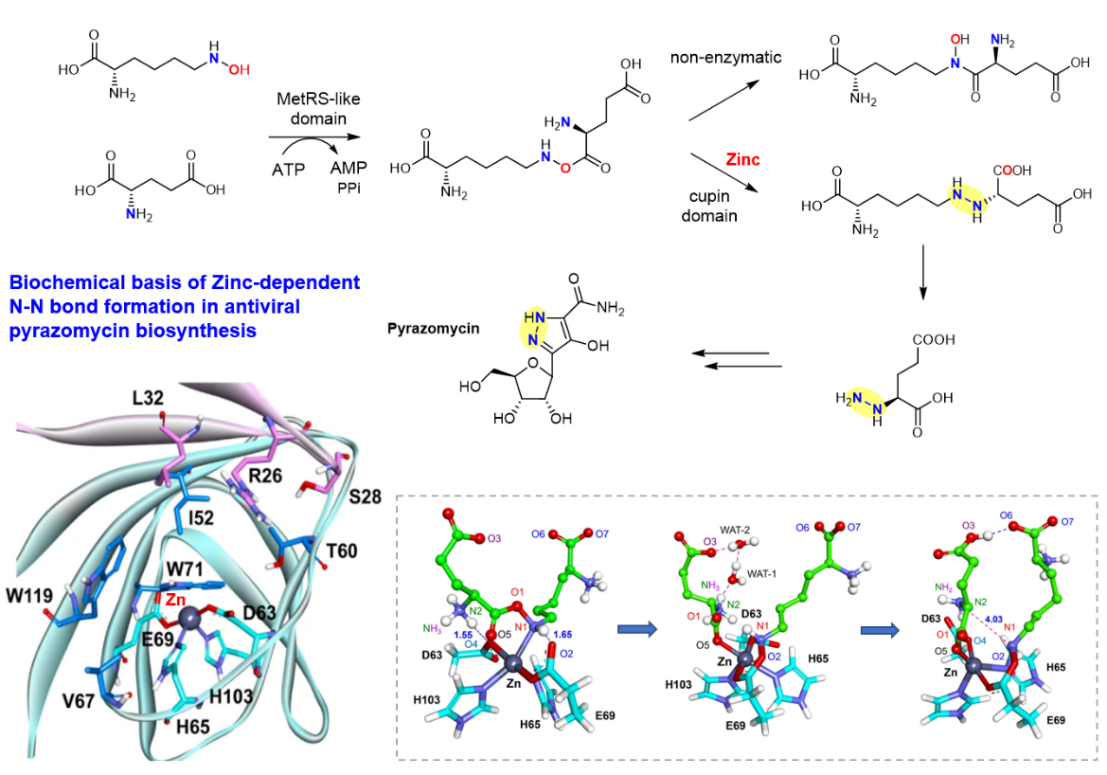
在本文中,研究者通过同位素示踪、体外生物化学反应重构、反应中间体结构鉴定等方法,揭示了在吡唑霉素生物合成过程中,双功能域蛋白PyrN的类似于氨酰-tRNA合成酶的C末端结构域(MetRS-like domain)能够利用ATP激活谷氨酸形成谷氨酰腺苷酸,后者继而与羟化赖氨酸缩合形成一个高度不稳定的酯中间体(图2)。PyrN的N末端Cupin结构域能够捕获该活性中间体,并将其转化为含有氮-氮(N-N)键连接的产物。在PyrN的cupin结构域缺失的情况下,由C末端结构域产生的活性酯中间体会在溶液中迅速发生自发的分子内重排形成含有酰胺键的副产物。进一步的蛋白结构分析、关键氨基酸残基定点突变与理论化学计算分析表明该新颖氮-氮(N-N)键的酶促合成反应严格依赖于Cupin结构域中结合的锌离子与关键的天冬氨酸残基Asp69。在以上两者的协同作用下,酯中间体在酶活性中心发生氮-氧(N-O)键断裂后重新形成氮-氮(N-N)键。此外,本文还通过蛋白质数据库挖掘和酶活测定,发现了多个能够接受不同氨基酸底物的该氮-氮键合酶家族的新成员,提示了本研究报道的氮-氮(N-N)键合成的生化反应是自然界普遍存在的一种微生物合成代谢策略(图3)。
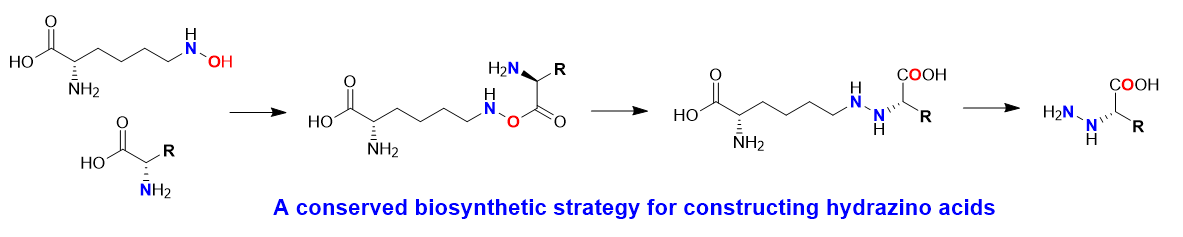
综上,本研究报道了一种普适性的锌离子依赖型氮-氮键基团酶促合成的生物化学反应过程,揭示了微生物合成代谢过程的一种新的生化机制。同时,鉴于氮-氮键基团是众多临床药物分子的关键药效团,该成果也将为通过合成生物学技术构筑相关药物分子提供催化元件和理论指导。
本文的第一作者为浙江大学杜艺岭课题组的博士生赵桂云和厦门大学化学化工学院王斌举教授课题组的博士生彭炜。论文主要通讯作者为杜艺岭研究员,共同通讯作者王斌举教授为该研究提供了理论化学计算的支持。该工作受到国家自然科学基金委项目和浙江省自然科学基金项目的支持。
原文链接:https://www.nature.com/articles/s41467-021-27523-x
杜艺岭课题组长期招聘微生物合成生物学、天然产物化学和结构生物学的博士后与研究助理(课题组网站:http://person.zju.edu.cn/yiling_du),欢迎邮件交流(yldu@zju.edu.cn)。
图文|杜艺岭课题组
编辑|郭静娴










